お手元で本コラムをご覧になりたい方は、こちらからダウンロードいただけます
 医薬製造におけるITの活用についてどのようなイメージをお持ちでしょうか。
医薬製造におけるITの活用についてどのようなイメージをお持ちでしょうか。
医薬製造の現場では、ロボット・カメラシステムなどの活用が包装・検査といった工程で進んでいますが、製造プロセスではまだまだ労働集約的な作業環境というのが一般的ではないかと思います。作業指示や作業記録といった製造情報も手書きでの入力が多く、先進・先端技術を活用した製品開発のイメージとは裏腹に、未だにアナログな生産実態なのではないでしょうか。製造品目の身体への影響や、製造ロットの単位を考えると、工程に熟知した作業者がフレキシブルに対応している現状をいかに変えていくか、というチャレンジをされているのでは、と思います。
本稿では、医薬品製造業におけるITの活用について、医薬品製造を取り巻く環境の理解を踏まえ、クリアすべき課題を具体化し、今必要とされる対応について整理していきたいと思います。医薬製造においては、法令遵守は当然ながら、基本的にはいかに自社のリスクに応じた対応をとるかということが重要です。その対応手段としてのITの活用について、その勘所と強化ポイントについて解説します。
第1回では、医薬品を取り巻く環境について俯瞰するとともに、重点となるGMPの発想における管理の考え方、ポイントについて述べたいと思います。
 医薬品製造に関する最近の動向として、小林化工株式会社の件を確認しておきましょう。
医薬品製造に関する最近の動向として、小林化工株式会社の件を確認しておきましょう。
事案の詳細は各報道に譲るとして、製薬会社では最長となる116日間の業務停止を受けました。このような違反に対する当局の理解を確認しておきましょう。図1に当局の議事情報の抜粋を記載しています。要因としては太字で示したようなポイントが読み取れ、自社でもこうした事象起きないか、という点検をしたくなります。
しかし、こうした「点」の確認は結果的には対応する必要はありますが、課題を設定するためには、赤字で示したような当局の対応の方向性としての「リスクの高い」「立入検査」「GMP調査体制の強化」について正しく理解し、それに必要な対応を整理する、という「線」や「面」での発想を持つことが重要と言えます。
当局は、具体的にどのような観点・考え方で「検査」や「強化」を図っていくのでしょうか。また、「リスクの高さ」をどのように考えるのでしょうか。
これらについては、隠されたノウハウというわけではなく、PMDA(Pharmaceuticals and Medical Devices Agency:独立行政法人医薬品医療機器総合機構)などの様々な開示情報の中で、繰り返し述べられていることを踏まえて想定すればよいでしょう。ここでは、GMPの管理に関して、可能な限りシンプルにその考え方を整理したものを図2にまとめました。
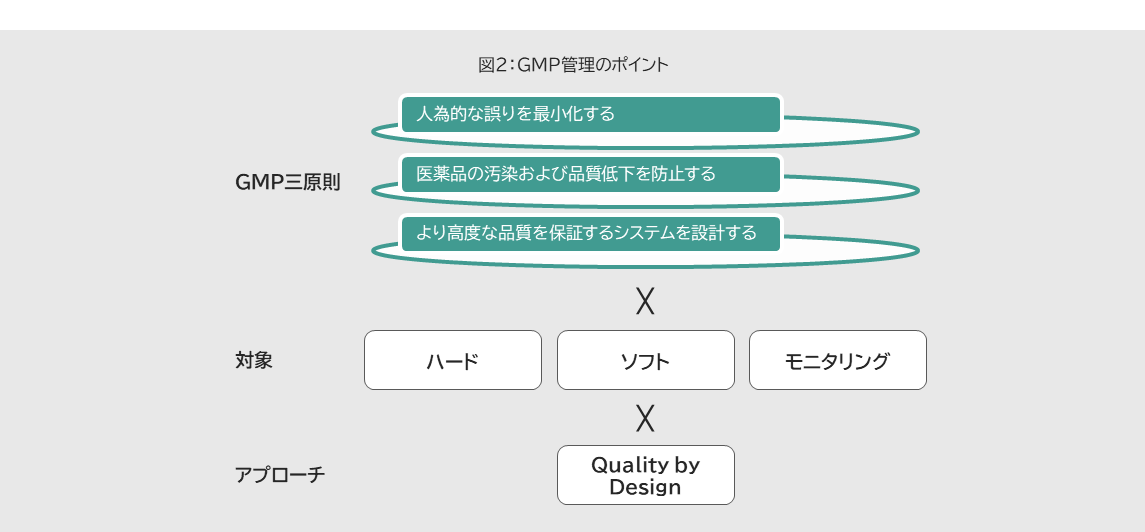
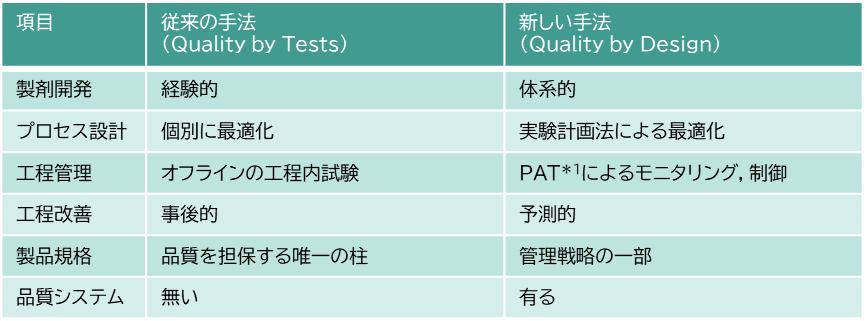
要素としては、GMP三原則をどの対象で具体的に展開しているのか、を整理します。その際に、アプローチとしてQuality by Design(QbD:リスク管理と科学を取り入れた, 製品ライフサイクル全体に適用可能な調和された品質システム)という理解のもと、必要な管理機能を検討するとよいでしょう。具体的なアプローチの内容は図3で項目別にキーワードで示すにとどめますが、新しい手法でのアプローチが実践できているか、を確認することが重要です。
図3:医薬品の製剤開発,品質管理における新旧アプローチの比較
*1:PAT(Process Analytical Technology)…プロセス解析工学
香取典子(2017) ファルマシア Vol. 53 No. 5 より一部抜粋、表記修正
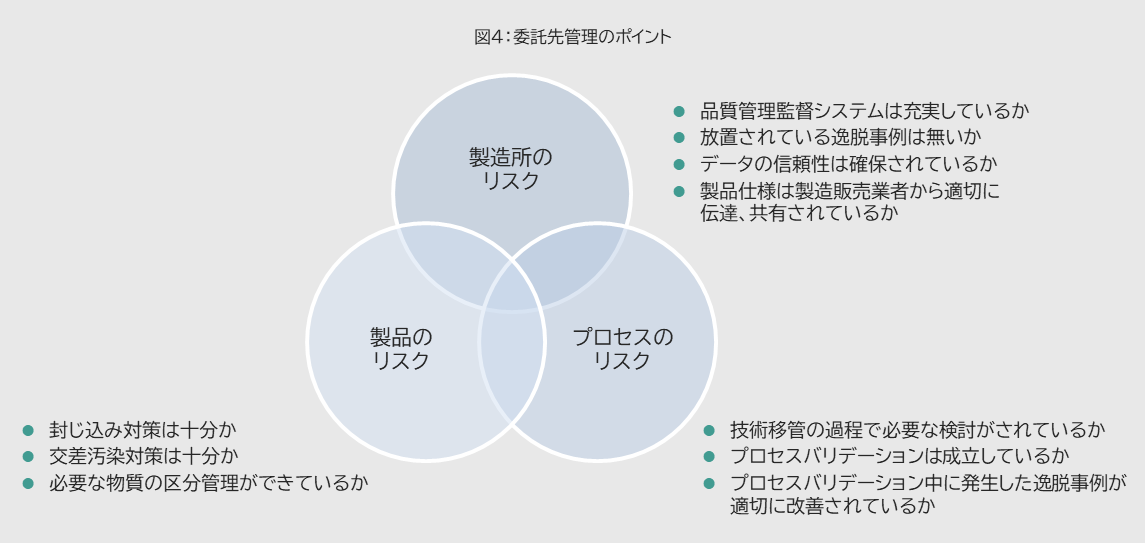
また、別の観点として、製造販売業者と製造所の役割分担を意識した、委託先管理が求められています。具体的には、図4で示すリスクを考慮したポイントになります。
これらを踏まえた検討として、例えば「(特定物質の)封じ込め対策」に関して言えば、以下のような整理ができます。
●ハード
- どのレベルで封じ込めを実現する製造設備、構造設備であるか
- 封じ込めるための機能を有しているか
- 排気ラインから漏れ出るリスクはないか
●ソフト
- 製造記録、一次容器、作業員に付着した物質が製造棟内外に拡散するリスクはないか
- 除去手順、更衣手順は適切か
●モニタリング
- 製造棟内外に拡散していないことを定期的にモニタリングしているか
- モニタリングの手法、検出方法等は適切か
- 結果として、封じ込められているか
こうした確認をするにあたり、人による作業ミスが起きないか、予測的な検討ができているか、といったような観点で業務の内容を点検してくことが重要ということです。
ITシステムの導入にむけて、他社での課題を「点」として取り込むのではなく、上記のような管理の枠組みや考え方を踏まえ、対応すべきリスクをどの業務でどんなアプローチで対応する必要があるのか、を見定めて課題を具体化することが本質的に対応につながるといえるでしょう。その課題を具体的に解決する手段として、ITがどのような貢献をするのか、を経営陣にアピールしていくことが重要です。
本稿では医薬品製造業におけるITの活用について、医薬品製造を取り巻く環境の理解を踏まえ、クリアすべき課題を具体化し、今必要とされる対応について述べてきました。
- 他社の課題や当局の指摘事項を「点」でとらえず、今後必要とされる管理のポイントを想定することが重要
- 管理のポイントとしては、GMP3原則を、ハード・ソフト・モニタリングの観点で明確化する
- リスクを検討する際には、Quality by Designのアプローチを踏まえ、必要な業務機能を設定すること
以上がサマリーとなります。
第2回では、こうした課題認識の下、具体的な強化の方向性とITの活用余地について探っていくことにします。
関連資料
医薬品製造業向け品質管理システム Expert LiMS (エキスパート リムス)
- GMPの国際基準(PIC/S GMP)が求める高水準の品質管理・品質保証体制の確立に向けた業務の標準化
- 試験データ一元管理、「ER/ES指針*1・Part11」、データインテグリティ(データの完全性)の適合をサポート
*1: Electronic Records/Electronic Signatures
→医薬品等の承認または許可等に係る申請などにおける、電磁的記録および電子署名の利用のための指針
執筆者プロフィール
島崎 里史(しまざき さとし)氏 E-mail : satoshi_shimazaki@jmac.co.jp
株式会社日本能率協会コンサルティング シニア・コンサルタント
生産コンサルティング事業本部 プロセス・デザイン革新センター
経歴
2003年3月 東京都立大学 理学研究科 修了
2007年12月 日本能率協会コンサルティング(JMAC)入社
2013年4月 チーフ・コンサルタント
2021年4月 シニア・コンサルタント
製造業を中心に、主に品質改善および生産性向上のコンサルティングを実施している。品質・原価の同時実現を競争力の源泉とする改革実現にむけた改善推進が得意。食品製造業での経験を活かし、フードチェーン全体の改革の必要性を感じ、農業から食品製造、流通小売におけるコンサルティングを推進中。農林水産省の食品製造業におけるイノベーション事業の責任者を複数年経験。
主なテーマは、食品製造業における生産システム・工程改善、品質管理強化、品質保証の仕組みづくりなど経営改革、生産性向上、作業効率化、収益改善、人材育成、研修などを中心に、コンサルティングを展開中。
【主な著書・論文等】
- JMA 生産マイスター(品質軸) 1・2級執筆、スクーリングテキスト編集
- JMA 通信教育テキスト(QC改善コース) 執筆
- JMA研修 品質保証セミナー、IE基礎テクニックコースなど
- 「開発プランニング 5Steps開発のフロントローディングに向けた仕掛け」(研究開発リーダー)


 医薬製造におけるITの活用についてどのようなイメージをお持ちでしょうか。
医薬製造におけるITの活用についてどのようなイメージをお持ちでしょうか。 医薬品製造に関する最近の動向として、小林化工株式会社の件を確認しておきましょう。
医薬品製造に関する最近の動向として、小林化工株式会社の件を確認しておきましょう。